Впервые получена трехмерная структура природной тетрамерной бутирилхолинэстеразы человека. Консорциум российских ученых, в состав которой вошли сотрудники ФИЦ Биотехнологии РАН, решили важную экспериментальную задачу, остававшуюся неразрешимой последние несколько десятилетий. Результаты проведенных исследований подробно описаны в статье международного научного журнала Biochimie, получившей в 2019 году премию журнала за лучшую статью года (Article of the Year Award).
 Российские ученые при поддержке Российского научного фонда впервые установили трехмерную структуру природной тетрамерной бутирилхолинэстеразы человека (БХЭ), решив тем самым важную экспериментальную задачу, остававшуюся неразрешимой последние несколько десятилетий.
Российские ученые при поддержке Российского научного фонда впервые установили трехмерную структуру природной тетрамерной бутирилхолинэстеразы человека (БХЭ), решив тем самым важную экспериментальную задачу, остававшуюся неразрешимой последние несколько десятилетий.
Авторами работы является коллектив ученых из ФИЦ Биотехнологии РАН, НИЦ «Курчатовский институт», ИБХФ РАН, Казанского университета, ФНИЦ «Кристаллографии и фотоники» РАН и ESRF (Франция). Помимо фундаментального значения полученные данные важны для разработки стратегий улучшения стабильности БХЭ и ее фармакокинетических свойств – ключевых характеристик для медицинского и биотехнологического использования данного фермента, в том числе, в качестве биоловушки (bioscavenger) при отравлениях фосфорорганическими соединениями.
Сотрудники ФИЦ Биотехнологии РАН координировали работы в рамках проводимого исследования, принимали участие в эксперименте по криоэлектронной микроскопии и реконструкции трехмерной структуры природной тетрамерной БХЭ человека.
Результаты проведенных исследований подробно описаны в статье международного научного журнала Biochimie «3D structure of the natural tetrameric form of human butyrylcholinesterase as revealed by cryoEM, SAXS and MD», получившей в 2019 году премию журнала за лучшую статью года (Article of the Year Award). Первый автор статьи – к.б.н. Константин Бойко, старший научный сотрудник лаборатории инженерной энзимологии ФИЦ Биотехнологии РАН.
 Бутирилхолинэстераза и ацетилхолинэстераза (АХЭ) являются структурно близкими ферментами, относящимися к классу сериновых гидролаз. Физиологическая роль АХЭ — регуляция уровня нейротрансмиттера ацетилхолина, была определена почти сто лет назад, при этом физиологическая роль БХЭ оставалась невыясненной до последнего времени. В головном мозге и в нервно-мышечных соединениях БХЭ может дублировать функции АХЭ, имея при этом важное токсикологическое и фармакологическое значение для организма, благодаря способности гидролизовать различные сложные эфиры, включая лекарственные (аспирин, ацетилированные пролекарства, и др.), наркотические (героин, кокаин, и др.) и отравляющие (зарин, зоман, VX, и др.). Это свойство открыло широкий спектр возможных применений БХЭ, в том числе в качестве самостоятельного биофармацевтического препарата и как модели для разработки систем защиты АХЭ и холинергической системы от отравления фосфоорганическими соединениями (ФОС), биомаркера для диагностики ФОС, в качестве компонента терапии наркозависимости, в качестве потенциальной терапевтической мишени для терапии болезни Альцгеймера и др.
Бутирилхолинэстераза и ацетилхолинэстераза (АХЭ) являются структурно близкими ферментами, относящимися к классу сериновых гидролаз. Физиологическая роль АХЭ — регуляция уровня нейротрансмиттера ацетилхолина, была определена почти сто лет назад, при этом физиологическая роль БХЭ оставалась невыясненной до последнего времени. В головном мозге и в нервно-мышечных соединениях БХЭ может дублировать функции АХЭ, имея при этом важное токсикологическое и фармакологическое значение для организма, благодаря способности гидролизовать различные сложные эфиры, включая лекарственные (аспирин, ацетилированные пролекарства, и др.), наркотические (героин, кокаин, и др.) и отравляющие (зарин, зоман, VX, и др.). Это свойство открыло широкий спектр возможных применений БХЭ, в том числе в качестве самостоятельного биофармацевтического препарата и как модели для разработки систем защиты АХЭ и холинергической системы от отравления фосфоорганическими соединениями (ФОС), биомаркера для диагностики ФОС, в качестве компонента терапии наркозависимости, в качестве потенциальной терапевтической мишени для терапии болезни Альцгеймера и др.
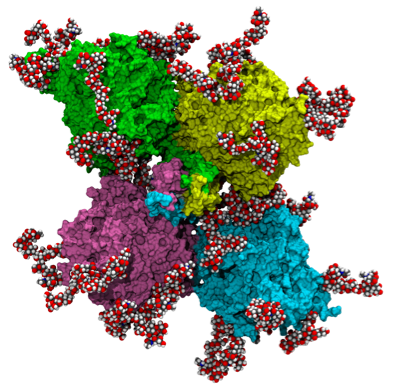
В плазме крови БХЭ существует в виде нескольких молекулярных форм, основной из которых (около 90% активности фермента) является тетрамер массой 340 кДа, организованный весьма сложным образом и имеющий крайне высокий процент гликозилирования (около 25% по массе) — 36 высокоподвижных гликановых цепей смешанного типа, связанных с остатками аспарагина на поверхности тетрамера белка.
Ранее методом рентгеноструктурного анализа было установлено более 50 структур частично дегликозилированной мономерной формы БХЭ человека, включая свободный фермент, комплексы с различными лигандами и конъюгаты с необратимыми ингибиторами. Однако все попытки получить кристаллы природного человеческого тетрамера БХЭ, проводившиеся в последние 30 лет, потерпели неудачу. Предполагается, что основной причиной является гликозилирование фермента, препятствующее правильной упаковке белка в кристалле. Ранее было проведено компьютерное моделирование структуры тетрамерной БХЭ, однако экспериментальных доказательств этой модели не существовало.
Установить структуру тетрамерной формы природной БХЭ удалось с использованием трех комплементарных методов — криоэлектронной микроскопии, молекулярной динамики и малоуглового рентгеновского рассеяния с привлечением расчетных мощностей суперкомпьютеров СКЦ МГУ им. Ломоносова и НИЦ «Курчатовский институт». Первичная модель БХЭ была получена на основе данных криоэлектронной микроскопии (разрешение 7.6Å). Однако данная модель была не полной — в ней отсутствовали, в частности, остатки гликанов (вследствие их подвижности), не ясно было также положение некоторых боковых групп аминокислотных остатков. Оптимизировать модель удалось благодаря использованию метода молекулярной динамики, а окончательную верификацию полученной после оптимизации модели провели с использованием метода малоуглового рентгеновского рассеяния. Полученные данные позволили, в частности, установить существенные различия между экспериментальной структурой и предложенной ранее молекулярно-динамической моделью.
Konstantin M. Boyko, Timur N Baymukhametov, Yury M Chesnokov, Michael Hons, Sofya V Lushchekina, Petr V Konarev, Alexey V Lipkin, Alexandre L Vasiliev, Ph.D. Patrick Masson, Vladimir O Popov, Michail V Kovalchuk ”3D structure of the natural tetrameric form of human butyrylcholinesterase as revealed by cryoEM, SAXS and MD” Biochimie, 2019, 156, 196-205 https://doi.org/10.1016/j.biochi.2018.10.017